王明席医生的科普号
- 精选 3分割伽玛刀放射外科治疗1-5个脑转移瘤的回顾性研究
目的:评估两种分割间隔的分割伽玛刀治疗大型脑转移瘤的结果。 方法:回顾分析接受分割伽玛刀治疗的45名多发(1-5个脑转移病灶)脑转移瘤(最大直径≥ 2厘米或体积≥ 5 cm3)患者。分为两组(标准分割组n=25, 长分割组 n=27)。 结果:中位随访期为10.5个月(范围5-25)。标准分割组在6个月时的局部肿瘤控制率为88.9%,12个月时为77.8%,而长分割组在6个月和12个月时的局部肿瘤控制率为100%(p=0.023,对数秩检验)。在多变量分析中,分割方案和肿瘤体积是影响3分割伽玛刀治疗后局部肿瘤控制的唯一重要因素。 结论:长分割伽玛刀治疗对大型脑转移瘤可能是一种有效和安全的治疗选择。
王明席 副主任医师 医生集团-山东 线上诊疗科279人已读 - 精选 2期临床试验证实Dexpramipexole对脊髓侧索硬化安全、有效,但还需3期临床试验后才能上市
http://alsn.mda.org/news/dexpramipexole-phase-2-results-show-efficacy-alsNewly published data confirm that in a two-part phase 2 clinical trial, the experimental therapy dexpramipexole showed dose-related slowing of symptom progression and increased survival time in people with amyotrophic lateral sclerosis (ALS).The findings were published online Nov. 20, 2011, in Nature Medicine by principal investigator Merit Cudkowicz (director of the MDA/ALS Center at Massachusetts General Hospital in Boston and a member of MDA’s Medical Advisory Committee) and colleagues.Based on trial results, dexpramipexole seems to be unique in that it both improves survival and slows symptom progression, the investigators note in their report."To our knowledge, no other drug has shown a clinically significant effect in the decline of [function] in a properly controlled clinical trial, and no other study has shown effects on both function and mortality," they wrote. Riluzole (Rilutek) — the only drug presently approved for treatment of ALS — modestly extends life span but doesn't cause significant improvement in function.Phase 2 trial data reveal safety and efficacyIn the phase 2 trial, conducted at 20 U.S. study sites, trial participants were randomly assigned to treatment and control groups twice, essentially creating two separate double-blind, placebo-controlled studies.In the first part of the study, which lasted 12 weeks, 102 trial participants each received either 50 milligrams, 150 milligrams or 300 milligrams per day of dexpramipexole, or a placebo (fake drug).Ninety-two participants moved on to part 2 of the trial, in which they all received placebo for 30 days (called a "washout period"). They then were randomly assigned to one of two groups, one receiving 300 milligrams of dexpramipexole per day for 24 weeks, and the other receiving 50 milligrams per day. A total of 71 people completed all 24 weeks.Higher doses of dexpramipexole correlated with a slower rate of decline in function, based on the ALSFRS-R (ALS Functional Rating Scale — Revised), a widely used and validated measure of functional ability in ALS.In part 1 of the study, the rate of functional decline in the group receiving 300 milligrams of dexpramipexole was 31 percent lower than the rate of decline in the placebo group. In part 2, participants receiving 300 milligrams a day showed a 20.5 percent slower rate of functional decline compared to those in the 50-milligram group.Mortality for participants in the 300-milligram group was 68 percent lower than in the 50-milligram group during the 24-week active phase in part 2 of the study.Functional decline and mortality also were analyzed together using a Combined Assessment of Function and Survival (CAFS) test. Results indicated that the 300-milligram/day dose of dexpramipexole was significantly more effective (correlated with more favorable outcomes) than the 50-milligram/day dose.In both parts of the study, an oral dose of dexpramipexole was found to be safe and well-tolerated when taken twice daily by trial participants. A temporary reduction in the number of white blood cells (neutropenia) was seen in a few participants and will be monitored in future trials, the investigators say."Results from this phase 2 study demonstrate why we’re so enthusiastic about the rapid advance of dexpramipexole to a phase 3 trial," Cudkowicz said in a press release."EMPOWER," a large-scale, global phase 3 clinical trial of dexpramipexole in ALS is under way at study sites in 28 U.S. states and 10 other countries.Dexpramipexole: Development detailsPreliminary results for this trial were reported at the April 2010 American Academy of Neurology meeting in Toronto and at the 2009 International Symposium on ALS/MND in Berlin.Dexpramipexole, also known as (R+) pramipexole, was developed under the name KNS-760704 by drug discovery and development company Knopp Biosciences (then called Knopp Neurosciences) in Pittsburgh, Pa.The molecule’s chemical structure is the mirror image of Mirapex, a prescription drug approved for the treatment of Parkinson's disease and restless legs syndrome. The structural difference between the two molecules results in significantly different pharmacological effects.Dexpramipexole has demonstrated neuroprotective properties in multiple studies involving cell cultures and laboratory animals. It appears to work by improving the function and efficiency of cellular "energy factories" called mitochondria. In ALS, mitochondria experience a cell-damaging process called oxidative stress, a condition that can contribute to the death of nerve cells (motor neurons).Knopp Biosciences and Biogen Idec in Weston, Mass., have partnered to develop dexpramipexole as an experimental treatment for ALS. (See Biogen Idec and Knopp Neurosciences Announce License Agreement for Late-Stage ALS Drug Candidate.) Biogen Idec holds an exclusive worldwide license from Knopp to develop and commercialize the drug, with Knopp providing development support.Dexpramipexole received orphan drug status from the U.S. Food and Drug Administration in October 2007, and a “fast-track” designation in September 2009. Orphan drug status provides financial incentives for the development of drugs for rare diseases.Meaning for people with ALSStudy investigators suggest that the favorable results from the phase 2 study of dexpramipexole "strongly support" further testing of the drug in ALS.While these results are encouraging, they must be confirmed in a large-scale, phase 3 study. An 800-person multinational phase 3 study already is under way but is no longer recruiting new participants.Two positive phase 3 clinical trials typically are required to receive FDA marketing approval, but in some cases a single positive study is sufficient (particularly if the trial involves a large number of trial participants, consistent results across multiple study sites and statistically significant results).Substantial evidence of efficacy in the ongoing phase 3 study will move dexpramipexole closer to FDA approval for treatment of ALS.
王明席 副主任医师 医生集团-山东 线上诊疗科2519人已读 - 精选 对于立体定向放射外科应用于治疗多发脑转移瘤的常见错误认识-来自《多发性脑转移瘤放射外科治疗指南》
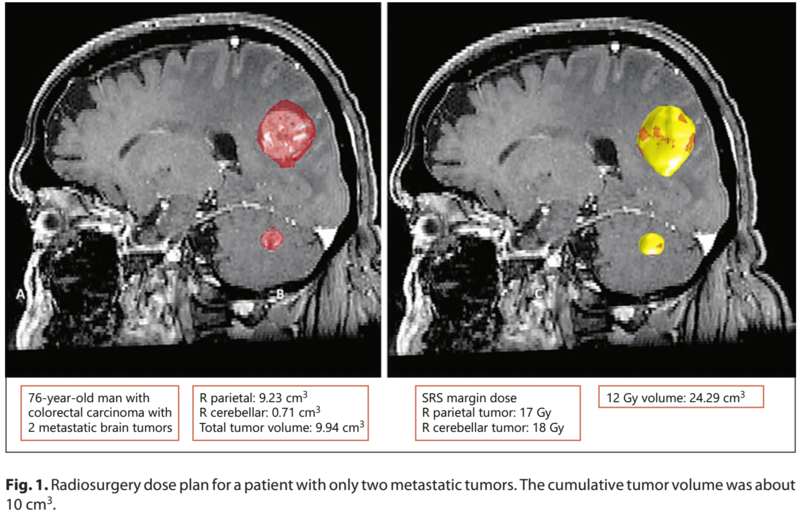
本文翻译自 《多发性脑转移瘤放射外科治疗指南》-2019年美国匹兹堡大学神经外科与放射肿瘤学科 (Prog Neurol Surg. 2019;34:100-109. doi: 10.1159/000493055.) 误解1:立体定向放射外科不能应用于超过10个肿瘤 现实 选择一定数量的肿瘤作为SRS合适的截止值,没有科学依据。目前的培训表明,肿瘤学家在决定脑转移瘤(BM)的立体定向放射外科(SRS)与全脑放射治疗(WBRT)的最佳治疗策略时,将病变数量作为一个重要考虑因素。许多实践中的放射肿瘤学家认为病灶数目是决定WBRT与SRS选择的最重要因素-比表现状态、病灶大小、累积肿瘤脑瘤负荷立方厘米、颅外疾病状态、组织学和患者便利性更重要(2)。然而,这种偏见没有科学依据。 最近的几项研究挑战了颅内BM的数量独立预测OS的假设。尽管在缺乏系统性疾病和脑肿瘤负担信息的情况下,颅内BM的数量可以预测生存率,但这部分是由于其与这些临床变量高度相关。具体而言,当纳入考虑这些其他变量的多变量模型时,颅内转移瘤的数量不能独立预测生存率。相反,正是这些疾病状态的替代指标与颅内转移相关。虽然很明显,系统性疾病负担和功能状态对决定生存率比颅内病变数量更重要,但颅内病变数量越高,生存率越差的概念通常用于选择SRS与WBRT的决策中。 一些研究表明,尽管病变数量是一个容易量化的指标,但它不一定是决定SRS最佳候选资格的最佳因素。肿瘤体积可能比病变数量更重要。Routman等人[10]表明,在未接受WBRT和/或手术的情况下接受SRS治疗的患者,单变量或多变量分析中病变数量不显著。他们报道肿瘤体积是一个重要因素。例如,与<10 cm3相比,肿瘤体积>10 cm3与更差的OS相关。先前的多个系列研究发现,在肿瘤体积增加和预后恶化之间的相关性方面,也有类似的结果。在本研究中,组织学和KPS(以及肿瘤体积)与OS显著相关。不幸的是,虽然病变数量通常是一个因素,但这些评分系统很少包括肿瘤体积[11]。为了进一步研究BM数量和体积相互作用的相关性,Routman等人[10]评估了两者之间的相关性,发现尽管BM数量的增加与肿瘤体积显著相关,但仅占方差的5%。 Ali等人[12]将BM数建模为一个连续变量,并逐步观察到,每增加6-7个 BM,死亡风险仅增加4%。这项研究表明,BM数量对生存率的贡献是有限的,因此BM数量不是最重要的因素,应该在更大的临床背景下考虑两者之间的决定SRS和WBRT。 在一项前瞻性观察试验(JLGK0901)中,患有2-4个BM(n=531)和5个或更多BM(n=208)的患者的平均生存期为10.8个月。两组的神经系统死亡或局部复发率没有差异[6]。一份日本报告包括778名1-10 BM患者,肿瘤总体积<15 cm3,他们符合前瞻性多研究所研究(JLGK0901)的标准,发现1、2、3-4、5-6或7-10脑损伤患者的OS没有差异。 在最近的一项研究中,Robin等人[14]报告了35名患者的结果,平均随访时间为4.1年。在一次SRS治疗中,BM的最大治疗个数为4至26个,在所有疗程中,BM的总治疗次数为4至47个(中位数为10个)。从诊断为BM开始,中位生存期为3.0年(ALK重排的NSCLC为4.2年;EGFR突变的NSCLC为2.4年),并且无论SRS疗程数、总共治疗的BM数或单个SRS疗程中治疗的BM数多少,生存期都是相似的。平均海马和全脑(WB)剂量非常低,即使是超过10个 BM(分别为1.2和0.8 Gy)接受治疗的患者。SRS治疗总体耐受性良好,5年无神经死亡率为84%。5年无WBRT治疗率为97%。Knoll等人[15]表明,在选定的BM较小的患者中,颅内转移>5例的患者在SRS方面总体效果良好,局部控制率良好,且治疗中无其他并发症。 其他几项研究最近也报道了类似的发现,这对颅内转移瘤数量作为独立预测指标的使用提出了挑战。Bhatnagar等人[16]和Baschnagel等人[17]先前的研究表明,肿瘤体积与总体生存率(OS)显著相关,而BM数量与OS无关。Likhacheva等人[18]最近报告了251名接受SRS进行BM初始治疗的患者,发现总肿瘤体积>2 cm3可预测OS,而BM数量不是OS的显著预测因子。 最终,决定用SRS治疗10个或10个以上肿瘤的患者取决于许多临床和病理因素,包括系统治疗选择、预后和患者的护理目标。如果可能,应与患者和家属讨论这些因素。肿瘤体积与其他临床和病理特征在预测方面可能比单纯的病变数量更重要,最近已被证明可以改善预后模型,包括疾病特异性GPA(分级预后评估)[19-21]。 误解2:全脑放疗治疗微转移,并显著降低神经系统死亡率 现实 “微转移”(在前MRI时代被定义为在缺乏足够高清晰度成像的情况下的可疑脑部疾病)的治疗通常被认为是提供WBRT而不是SRS的理由。一些医生认为,在10个以上转移的病例中,微转移的几率仍然很高,因此WBRT可能是这些患者的更好选择。然而,高分辨率MRI可以识别直径在2-3mm范围内的肿瘤。通过密切监测,SRS术后出现局部失败(由于未识别的微转移)的患者可以接受有效的SRS抢救、致残率低。 随着潜在对颅内转移灶的越来越有效的系统疗法的出现,WBRT在控制微转移中的应用受到了挑战。在Sahgal等人[4]的荟萃分析中,增加WBRT后神经系统死亡的风险从30%降低到25%。考虑到潜在的毒性,20名患者进行WBRT以防止另外的神经系统死亡是不合理的。与这一变化相一致,一个更现代的多机构前瞻性系列(JLGK0901)对1194名BM高达10的患者进行伽玛刀SRS治疗,无辅助WBRT,其神经系统死亡率仅为8%[6]。WBRT是否可以用于控制大脑中的显微镜下或隐匿性转移,现在是一个不太相关的问题,因为可以使用系统疗法。 误解3:立体定向放射外科治疗>10个转移瘤与大脑的高总平均和积分剂量相关 现实 支持SRS而非WBRT以保持生活质量的研究表明,较低的脑容积治疗可能是改善记忆和执行功能的机制。这似乎是一个自然的假设,随着大量脑损伤的治疗,治疗的脑体积也以线性方式增加。如果是这样的话,那么对SRS治疗的脑肿瘤数量进行限制将是合理的。然而,评估肿瘤数量和体积的研究没有发现支持这一假设的证据。 多发性脑转移患者的治疗已由WBRT转向SRS。然而,可能有人担心多发性转移SRS可能导致更高的脑辐射毒性。Hatiboglu等人[22]进行了一项分析,以研究肿瘤数量和体积在全脑平均剂量和积分剂量中的作用。本研究的目的是确定在治疗不同数量的靶点和病变体积时,脑辐射剂量的变化。这些作者用不同的肿瘤体积(包括0.1、0.5、1、2和5 cm3)和肿瘤数量(包括1、3、5、10、15、20和25)的不同组合模拟不同的治疗方案。使用Leksell GammaPlan?对患者头部的计算机断层扫描中的所有组合进行治疗计划。他们研究了低剂量(20和18Gy)和高剂量(24和20Gy)。在较低处方给药计划中,50%等剂量线给予边际剂量,当病灶数量小于15时使用20Gy,当病灶数量等于或大于15时使用18Gy。在更高的处方剂量表中,小于5 cm3的病变使用24 Gy的边际剂量,等于5 cm3的病变使用20 Gy。计算每个场景的平均WB剂量、WB积分剂量和接受12 Gy(V12 Gy)的大脑体积。他们的分析表明,肿瘤总体积比病变数量更能预测V12 Gy,并且发现肿瘤总体积与V12 Gy之间存在线性相关。他们还发现,与病变数量相比,肿瘤总体积是全脑平均剂量和全脑积分剂量的更重要预测因子。这项研究表明,单一伽玛刀SRS程序可以安全地治疗多个中小型病变。 Rivers等人[23]使用SRS评估了肿瘤数量对大脑总剂量的影响。治疗的病灶数量从1个到29个不等。肿瘤边缘的平均处方剂量为18gy。这些作者发现病变数量与大脑V8、V12、V10或V15之间没有相关性。治疗的脑体积(V8、V10、V12和V15)与治疗的肿瘤总体积之间存在直接且具有统计学意义的关系。在本研究中,只有当肿瘤总体积超过25 cm3时,对大脑的积分剂量才超过3.0 J。这(3 J)相当于2.4 Gy的总脑剂量,比WBRT的单次分割放疗剂量要小[23]。 采用传统的分割方案,一个完整的WBRT疗程可提供37.95 Gy的整体脑剂量。在这项研究中,总治疗肿瘤体积和观察到的积分剂量之间的关系是二次的。一种可能的解释是,较大或较多肿瘤患者处方剂量的体积依赖性减少。他们还报告说,对于符合性较高且梯度指数较低的计划,整体脑剂量明显较低,这表明计划质量和SRS技术可能对整体剂量产生重要影响,从而降低不良辐射影响的风险。因此,如果SRS的一个目标是保持正常的大脑功能,那么重点应该从病灶数量转移到目标病灶的总体积。 在作者中心,提供SRS的决定不仅仅基于肿瘤的数量。作者认为肿瘤在大脑中的累积体积是最重要的因素。?图1显示一名患者仅有2个肿瘤,肿瘤累积体积约为10 cm3。大多数医生会认为这个病人是一个很好的SRS候选人。较大肿瘤边缘剂量为17 Gy,较小肿瘤边缘剂量为18 Gy,总12 Gy体积为24.29 cm3。 与此相比,图2显示了一位有28个小病灶的患者。根据肿瘤的数量,一些医生不会认为她是一个很好的SRS候选人,而宁愿提供WBRT。然而,本例中的总估计脑肿瘤体积仅为2.7 cm3。所有28个肿瘤的边缘剂量均为16 Gy,总12 Gy体积为16 cm3。这些参数表明,该患者可能在SRS方面表现良好,应被视为比第一位患者更好的候选者。 在推荐SRS时考虑了几个因素。这些因素包括: 1患者年龄 2患者症状 3原发病情况 4是否存在其他器官转移 5患者目前的神经状态 6病人的身体状况 7估计累积肿瘤体积(脑肿瘤负担) 8肿瘤数量 9先前WBRT的历史 10以往脑部手术史 11患者对神经认知功能的关注和风险承受能力。 12基于知情同意的患者意愿和偏好。
 王明席 副主任医师 医生集团-山东 线上诊疗科341人已读
王明席 副主任医师 医生集团-山东 线上诊疗科341人已读 - 脑转移瘤的治疗新进展 《多发性脑转移瘤放射外科治疗指南》-2019年美国匹兹堡大学神经外科与放射肿瘤学科
避免全脑放射治疗的原因 以随机方式和荟萃分析[4]对全脑放射治疗(WBRT)与立体定向放射外科(SRS)的疗效和毒性进行了评估。最近的试验表明,在SRS中加入WBRT不会改善生存结果,并且WBRT会导致1-3 BM患者的神经认知和总体生活质量显著下降[5]。Alliance试验N0574随机选择了1-3例SRS脑转移患者与SRS合并WBRT患者,并发现中位总生存率(OS)无统计学显著差异。SRS后的WBRT改善了局部和区域控制,但对OS无影响,且与认知功能下降有关治疗3个月后,生活质量下降[5]。 许多患者在WBRT期间或之后不久会出现急性副作用,包括皮炎、脱发和疲劳。神经毒性被认为是在少数长期存活者中观察到的一种迟发效应。然而,最近的研究表明,在WBRT的3-6个月内可能出现神经认知功能(NCF)缺陷。NCF很重要,因为它可以预测生活质量、功能独立性和生存率。NCF的下降增加了护理者的负担,并损害了财务、工作和社会活动。WBRT还导致与疲劳、身体功能和角色功能相关的健康相关生活质量较差。 立体定向放射外科的优势 SRS单独或与其他方式相结合通常被认为是多发性脑转移患者的标准治疗方法。Yamamoto等人[6–8]记录了与BM较少的患者相比,SRS治疗4个或更多BM患者的等效结果。对于有5个或更多BM的患者,没有关于SRS与WBRT的公开随机试验。在缺乏1级证据解决多发转移患者的最佳治疗的情况下,如果SRS在治疗2-4个转移瘤方面比WBRT具有某些优势,那么对于10个或更多的转移瘤,SRS将继续具有这些优势,这是很直观的。 SRS除了高效和安全外,对患者及其家属还有其他一些优势。例如,SRS可以在单次治疗中执行,这是一个更方便患者的功能。相比之下,接受WBRT的患者需要中断系统治疗,因为每天的分割计划超过10-14个治疗日(跨度2-3周)。因此,与接受WBRT治疗的患者相比,接受SRS治疗的患者最终可能接受更多的系统性治疗WBRT[9]。在新的靶向药物时代,这是一个特别重要的考虑因素,可以显著影响生存和疾病负担。 SRS比WBRT有几个优点,包括几乎没有急性毒性。在一天内完成治疗有助于继续其他治疗(如化疗)。WBRT的潜在作用可用于粟粒性疾病进展或软脑膜受累的患者。此外,SRS允许保留尽可能多的正常脑组织,从而保护认知功能和生活质量。 本文翻译自 Prog Neurol Surg. 2019;34:100-109. doi: 10.1159/000493055.
王明席 副主任医师 医生集团-山东 线上诊疗科278人已读 - 脑转移瘤的治疗新进展 伽玛刀治疗15个以上脑转移瘤的结果-回顾性研究
背景:尽管有证据支持伽玛刀立体定向放射外科(SRS)的广泛应用,但安全有效地治疗转移瘤的数量仍然存在争议。我们致力于阐明首次SRS时出现≥ 15个脑转移灶的患者的生存结果。 方法:这项回顾性分析回顾了乳腺癌、肺癌或黑色素瘤引起的接受治疗的≥15脑转移患者。93名患者符合纳入标准。本研究共治疗3016例肿瘤。在第一次SRS手术中,乳腺癌的肿瘤中位数为23(范围15-67),肺癌为21(范围15-48),黑色素瘤为21(范围15-67)。乳腺、肺和黑色素瘤转移灶的平均总体积分别为8.75 cm3、6.89 cm3和9.98 cm3。 结果:乳腺癌、肺癌和黑色素瘤患者诊断脑转移后的中位生存期分别为18.0、9.4和6.3个月。SRS后乳腺癌的生存期为16个月,肺癌为4.6个月,黑色素瘤为3.1个月。SRS治疗后,乳腺癌患者的生存期明显长于肺癌和黑色素瘤患者(P=0.001)。较高的Karnofsky表现状态评分与所有肿瘤类型的生存率增加相关。对56%的乳腺癌患者、35%的肺癌患者和24%的黑色素瘤患者进行局部或远处进展重复SRS。 结论:SRS是治疗广泛脑转移的有效手段,尤其是乳腺癌患者。原发肿瘤类型、全身疾病和工作状态严重影响生存结果。 翻译的摘要来自 World Neurosurg. 2019 Jun;126:e989-e997. doi: 10.1016/j.wneu.2019.03.019
王明席 副主任医师 医生集团-山东 线上诊疗科323人已读 - 精选 两阶段伽玛刀放射外科治疗10个以上脑转移瘤的结果-脑转移灶数量不是生存期的决定因素
目的:尽管立体定向放射外科是治疗脑转移瘤的主要方法,但其治疗方法和疗效尚未明确。本研究旨在评估两阶段伽玛刀放射外科(GKS)治疗10个以上转移病灶的疗效。 患者和方法:当单次放射外科手术无法忍受或暴露的脑容量过大时,对诊断为多处转移的52例患者应用分期GKS。在第一次GKS中,对脑关键部位有临床意义的大型病变进行了治疗。其余病灶在4周内接受第二次GKS辐射。该研究评估了三个主要结果:1)第二次GKS和3个月随访时的放射反应,2)治疗相关副作用,以及3)分期GKS治疗后的生存率。 结果: 17例(32.7%)患者的受照病灶在第二次GKS时在MRI上显示放射反应。在同一时期,13名(25.0%)患者在首次GKS时未治疗的病变进展。在3个月的随访中,5例(9.6%)和7例(13.5%)患者分别部分缓解和稳定。考虑到一些患者在第三次随访前大多因非神经原因死亡,我们无法检测到无偏倚的影像学进展。52名患者中有9名(17.3%)在第二次GKS前出现1-3级毒性,而26名幸存者中有4名(15.4%)出现1-2级CNS毒性,但辐射与毒性之间的关系尚不清楚。52例患者在3、6、12、18和24个月时的生存率分别为63.9%、44.1%、23.3%、17.8%和13.3%。在分期GKS治疗后KPS ≥ 80而不是<70,RPA II而不是III,PIV<7000 mm3观察到患者更长的生存期。然而,大于或小于10个靶病变的数量与生存率无关。 结论:尽管本研究不能清楚地显示临床益处和生存增益,但两阶段GKS治疗多个转移瘤似乎有利于患者和避免风险。选定的患者,尤其是没有其他治疗方案的患者,可以作为该治疗方案的候选患者。 翻译的文摘来自Clin Neurol Neurosurg. 2020 Aug;195:105847. doi: 10.1016/j.clineuro.2020.105847.
王明席 副主任医师 医生集团-山东 线上诊疗科329人已读 - 精选 脑内多发、大型转移瘤的伽玛刀治疗、肿瘤复发和转移灶的免疫细胞治疗、慢性乙型肝炎的治疗性疫苗
1、开展多发、关键部位、直径>2cm(或体积>5cm3)的转移瘤的伽玛刀低分次治疗:有关回顾性研究提示,长间期低分割伽玛刀治疗1-5个脑转移治疗后12个月时的局部肿瘤控制率为100%;2、开展以肿瘤浸润T细胞为工具的自体免疫细胞治疗转移瘤临床研究:有关研究证实可以清除多发转移瘤,理论上可以预防未突变肿瘤的复发;3、恶性胶质瘤肿瘤的新治疗研究;4、开展慢性乙型肝炎的自体树突细胞治疗性疫苗的临床研究:有关临床研究已经证实较好的临床治疗效果。
王明席 副主任医师 医生集团-山东 线上诊疗科277人已读 - 进行性肌营养不良 SMT C1100(英国):做玩了I期临床试验,证实安全,但未发现有效,分析认为与剂型有关,II期试验缺乏资金开展。
SMT C1100(英国):做玩了I期临床试验,证实安全,但未发现有效,分析认为与剂型有关,II期试验缺乏资金开展。参见网站:http://www.summitplc.com/DMD-utrophin-upregulation.aspxhttp://www.parentprojectmd.org/site/PageServer?pagename=Advance_research_pipeline_smtc1100
王明席 副主任医师 医生集团-山东 线上诊疗科2493人已读 - 亨廷顿舞蹈病 《亨廷顿氏舞蹈症(Huntington's Disease)》或许以另外一种治疗方式
亨廷顿氏舞蹈症(Huntington's Disease)以另外一种治疗方式,本实验室计划表达纯化蛋白。但是临时缺乏资金。
王明席 副主任医师 医生集团-山东 线上诊疗科2222人已读 - 颞叶癫痫 用治疗克隆氏病的柳氮磺吡啶可能用来治疗胶质瘤引起的癫痫
Glutamate release by primary brain tumors induces epileptic activitySusan C Buckingham,1Susan L Campbell,1Brian R Haas,1Vedrana Montana,1Stefanie Robel,1Toyin Ogunrinu1& Harald Sontheimer1AffiliationsContributionsCorresponding authorJournal name:Nature MedicineVolume:17,Pages:1269–1274Year published:(2011)DOI:doi:10.1038/nm.2453Received05 May 2011Accepted27 July 2011Published online11 September 2011AbstractAbstractAuthor informationSupplementary informationArticle tools日本語要約PrintEmailDownload citationOrder reprintsRights and permissionsShare/bookmarkConnoteaCite U LikeFacebookTwitterDeliciousDiggEpileptic seizures are a common and poorly understood comorbidity for individuals with primary brain tumors. To investigate peritumoral seizure etiology, we implanted human-derived glioma cells into severe combined immunodeficient mice. Within 14–18 d, glioma-bearing mice developed spontaneous and recurring abnormal electroencephalogram events consistent with progressive epileptic activity. Acute brain slices from these mice showed marked glutamate release from the tumor mediated by the system xc cystine-glutamate transporter (encoded by Slc7a11). Biophysical and optical recordings showed glutamatergic epileptiform hyperexcitability that spread into adjacent brain tissue. We inhibited glutamate release from the tumor and the ensuing hyperexcitability by sulfasalazine (SAS), a US Food and Drug Administration–approved drug that blocks system xc. We found that acute administration of SAS at concentrations equivalent to those used to treat Crohn's disease in humans reduced epileptic event frequency in tumor-bearing mice compared with untreated controls. SAS should be considered as an adjuvant treatment to ameliorate peritumoral seizures associated with glioma in humans.
王明席 副主任医师 医生集团-山东 线上诊疗科1125人已读





